pH测量偏差的利与弊,您知道吗?
pH值作为一个重要的理化指标,在我们的日常生活、工农业生产制造过程中无处不在。
根据《生活饮用水水质准则》规定:饮用水的pH范围为6.5-8.5;
•生物制药中细菌发酵、细胞培养过程,只有在特定的pH环境中细菌/细胞才具有最佳生长速率,从而获得最佳收益;
•瓶装啤酒的pH控制在3.9-4.1之间,以提高存放的稳定性;
•锂电正极材料制备时,需控制pH值在11.0左右,以获得质量最佳的产品;
•火电工业标准要求锅炉补给水的pH控制在8.5-9.3,以降低对设备的腐蚀、确保生产安全。

但在实际应用中,由于pH电极老化,操作或维护不当等原因,常会产生不同程度的测量偏差。那么,pH测量偏差会对过程产生什么样的影响呢?
被“低估”的氢离子浓度误差
pH值被定义为氢离子活度的负对数,
pH= -log[αH+]
因此,pH值的变化直接反映了氢离子活度的变化,此处活度约等于浓度。
pH值和氢离子浓度间的关系如下图所示,从图中可以算出:pH值偏差0.1,氢离子浓度差超过20%;pH值偏差0.5,氢离子浓度差超过3倍。
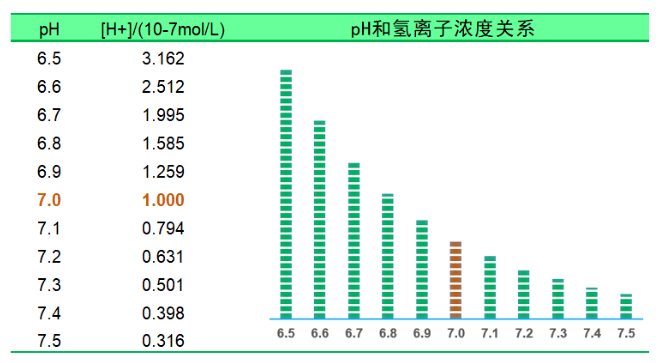
对于有[H+]或[OH-]参与的反应过程,氢离子浓度偏差将会影响反应过程和产品质量。因此,有必要从实际工艺出发,充分考量过程控制中pH的精确性。
例如,青霉素发酵的最适pH值在6.8左右,若测量电极存在误差,会影响产品的生产效率;同时,由于青霉素是一种有机弱酸,pH超过7有可能使青霉素水解,造成严重的经济损失。
pH测量偏差会造成原料浪费
pH测量偏差还可能造成原料浪费,下图使用0.01M的NaOH溶液将0.01M HCl溶液的pH值从2.0调节到3.0。
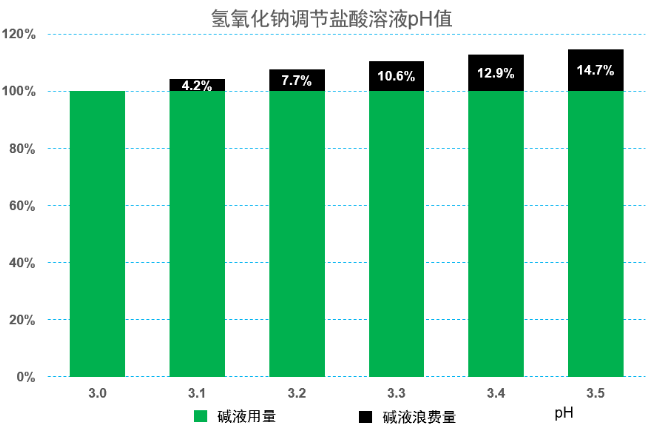
从图中可以看出,pH偏高0.5时(实际值为3.5),NaOH用量比准确值高出14.7%;对每周耗碱量为1t的某企业而言,就意味着每年会产生7.6t的碱原料 (NaOH,4000RMB/t) 的浪费,仅由于碱增加的处理成本就高达3万元。
同时,对许多企业而言,生产中常产生大量的废水,由于环保要求,排放前需调节pH至排放标准。但废水的组成一般都较为复杂,水处理过程往往并不是简单地酸碱中和。
pH测量至关重要
对于含有重金属离子的废水,常需要控制pH分步沉淀出相应的重金属离子;


在这种情况下,pH偏差会同时造成沉淀剂用量的增加,甚至会使原本已沉淀的重金属离子络合水解返溶到溶液。
例如,在使用硫化钠(Na2S)处理含汞废水时,控制pH为9~10可完全去除含汞有害物。若pH值产生0.5的偏差至10.5,则Na2S的用量将增加一倍,且有部分已沉淀出来的汞离子将返溶到溶液中,导致原料成本增加30%,且企业面临环境污染的风险。
若溶液中含有仅能部分电离的弱酸或弱碱,弱酸/弱碱就会与其对应的盐组成缓冲体系,进一步阻碍pH变化,加大pH调节的难度。在缓冲体系下调节pH需消耗较多的酸或碱,pH偏差即会引起较为显著的酸碱浪费。
综上,pH测量偏差使过程工艺偏离最优的控制点,进而影响产品质量、造成原料浪费,严重的甚至还会酿成生产事故。因此,精确可靠的pH测量对许多工艺点至关重要。
pH测量

经过70余年的发展,梅特勒-托利多在pH测量方面积累了十分丰富的研发和应用经验,可提供最精确可靠的pH测量,为您的生产过程保驾护航 !










